Karbon adalah salah satu unsur yang paling biasa dalam alam semula jadi, merangkumi sifat-sifat hampir semua bahan yang terdapat di Bumi. Ia mempamerkan pelbagai ciri, seperti kekerasan dan kelembutan yang berbeza-beza, kelakuan penebat-semikonduktor-superkonduktor, penebat haba-superkonduktiviti, dan ketelusan lengkap penyerapan cahaya. Antaranya, bahan dengan penghibridan sp2 adalah ahli utama keluarga bahan karbon, termasuk grafit, tiub nano karbon, graphene, fullerene, dan karbon berkaca amorf.
Sampel Grafit dan Karbon Berkaca
Walaupun bahan-bahan sebelum ini terkenal, mari kita fokus pada karbon berkaca hari ini. Karbon kaca, juga dikenali sebagai karbon kaca atau karbon vitreus, menggabungkan sifat kaca dan seramik menjadi bahan karbon bukan grafit. Tidak seperti grafit kristal, ia adalah bahan karbon amorfus yang hampir 100% sp2-hibrid. Karbon berkaca disintesis melalui pensinteran suhu tinggi bagi sebatian organik prekursor, seperti resin fenolik atau resin alkohol furfuryl, di bawah suasana gas lengai. Penampilannya yang hitam dan permukaan licin seperti kaca menjadikannya nama "karbon berkaca."
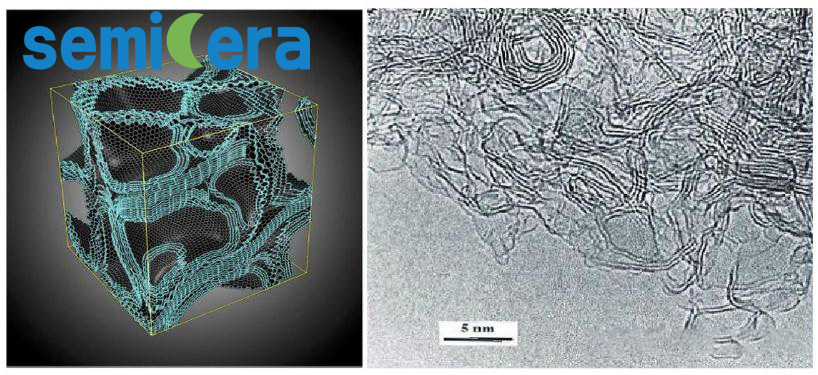
Sejak sintesis pertamanya oleh saintis pada tahun 1962, struktur dan sifat karbon berkaca telah dikaji secara meluas dan kekal menjadi topik hangat dalam bidang bahan karbon. Karbon berkaca boleh dikelaskan kepada dua jenis: Karbon berkaca Jenis I dan Jenis II. Karbon kaca jenis I disinter daripada prekursor organik pada suhu di bawah 2000°C dan terdiri terutamanya daripada serpihan grafena bergulung berorientasikan rawak. Karbon kaca jenis II, sebaliknya, disinter pada suhu yang lebih tinggi (~2500°C) dan membentuk matriks tiga dimensi berbilang lapis amorfus struktur sfera seperti fullerene yang dipasang sendiri (seperti yang ditunjukkan dalam rajah di bawah).
Perwakilan Struktur Karbon Berkaca (Kiri) dan Imej Mikroskopi Elektron Beresolusi Tinggi (Kanan)
Penyelidikan terkini mendapati bahawa karbon berkaca Jenis II mempamerkan kebolehmampatan yang lebih tinggi daripada Jenis I, yang dikaitkan dengan struktur sfera seperti fullerene yang dipasang sendiri. Walaupun terdapat sedikit perbezaan geometri, kedua-dua matriks karbon berkaca Jenis I dan Jenis II pada asasnya terdiri daripada graphene bergulung yang tidak teratur.
Aplikasi Karbon Kaca
Karbon berkaca mempunyai banyak sifat yang luar biasa, termasuk ketumpatan rendah, kekerasan tinggi, kekuatan tinggi, kebolehtelapan tinggi kepada gas dan cecair, kestabilan haba dan kimia yang tinggi, yang menjadikannya boleh digunakan secara meluas dalam industri seperti pembuatan, kimia dan elektronik.
01 Aplikasi Suhu Tinggi
Karbon berkaca mempamerkan rintangan suhu tinggi dalam gas lengai atau persekitaran vakum, menahan suhu sehingga 3000°C. Tidak seperti bahan suhu tinggi seramik dan logam yang lain, kekuatan karbon berkaca meningkat dengan suhu dan boleh mencapai sehingga 2700K tanpa menjadi rapuh. Ia juga mempunyai jisim yang rendah, penyerapan haba yang rendah, dan pengembangan haba yang rendah, menjadikannya sesuai untuk pelbagai aplikasi suhu tinggi, termasuk tiub perlindungan termokopel, sistem pemuatan dan komponen relau.
02 Aplikasi Kimia
Oleh kerana rintangan kakisannya yang tinggi, karbon berkaca banyak digunakan dalam analisis kimia. Peralatan yang diperbuat daripada karbon berkaca menawarkan kelebihan berbanding radas makmal konvensional yang diperbuat daripada platinum, emas, logam tahan kakisan lain, seramik khas atau fluoroplastik. Kelebihan ini termasuk rintangan kepada semua agen penguraian basah, tiada kesan ingatan (penjerapan tidak terkawal dan desorpsi unsur), tiada pencemaran sampel yang dianalisis, rintangan kepada asid dan cair alkali, dan permukaan berkaca yang tidak berliang.
03 Teknologi Pergigian
Crucible karbon berkaca biasanya digunakan dalam teknologi pergigian untuk mencairkan logam berharga dan aloi titanium. Mereka menawarkan kelebihan seperti kekonduksian terma yang tinggi, jangka hayat yang lebih lama berbanding mangkuk pijar grafit, tiada lekatan logam berharga cair, rintangan kejutan haba, kebolehgunaan untuk semua logam berharga dan aloi titanium, penggunaan dalam emparan tuangan aruhan, penciptaan atmosfera pelindung ke atas logam cair, dan penghapusan keperluan untuk fluks.
Penggunaan mangkuk pijar karbon berkaca mengurangkan masa pemanasan dan lebur dan membolehkan gegelung pemanas unit lebur beroperasi pada suhu yang lebih rendah daripada bekas seramik tradisional, dengan itu mengurangkan masa yang diperlukan untuk setiap tuangan dan memanjangkan jangka hayat pijar. Selain itu, ketidakbolehbasahannya menghapuskan kebimbangan kehilangan bahan.
04 Aplikasi Semikonduktor
Karbon berkaca, dengan ketulenannya yang tinggi, rintangan kakisan yang luar biasa, ketiadaan penjanaan zarah, kekonduksian, dan sifat mekanikal yang baik, adalah bahan yang sesuai untuk pengeluaran semikonduktor. Crucible dan bot yang diperbuat daripada karbon berkaca boleh digunakan untuk zon lebur komponen semikonduktor menggunakan kaedah Bridgman atau Czochralski, sintesis galium arsenide, dan pertumbuhan kristal tunggal. Selain itu, karbon berkaca boleh berfungsi sebagai komponen dalam sistem implantasi ion dan elektrod dalam sistem etsa plasma. Ketelusan sinar-Xnya yang tinggi juga menjadikan cip karbon berkaca sesuai untuk substrat topeng sinar-X.
Kesimpulannya, karbon berkaca menawarkan ciri-ciri luar biasa yang termasuk rintangan suhu tinggi, lengai kimia dan prestasi mekanikal yang sangat baik, menjadikannya sesuai untuk pelbagai aplikasi dalam pelbagai industri.
Hubungi Semicera untuk produk karbon kaca tersuai.
e-mel:sales05@semi-cera.com
Masa siaran: Dis-18-2023